
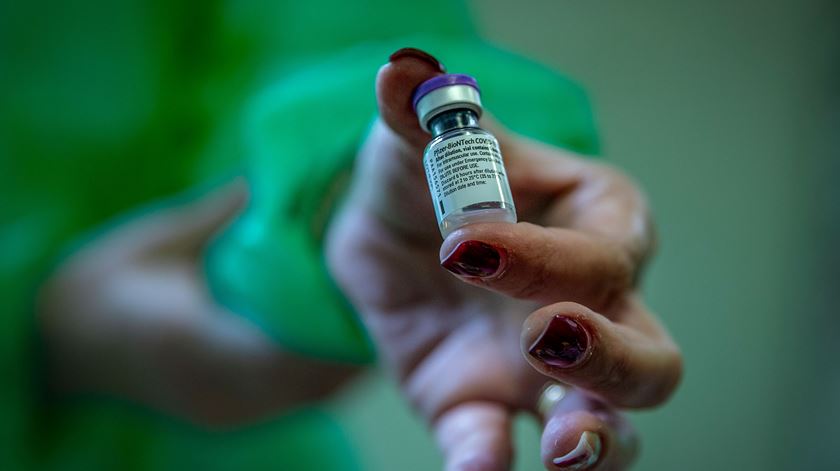
Os consultores do regulador norte-americano para a saúde (Food and Drug Administration – FDA) aprovaram a recomendação de uso de emergência da vacina Covid-19 da Pfizer em crianças entre os 5 e os 11 anos.
A votação ocorreu na terça-feira e obteve 17 votos a favor, nenhum contra e uma abstenção.
“Consideramos ter otimizado a resposta imunológica e minimizámos as reações”, sustentou o vice-presidente sénior da Pfizer, William Gruber, na reunião com os consultores.
Mas, se muitos membros do Comité Consultivo de Vacinas e Produtos Biológicos Relacionados da FDA concordaram que os benefícios da vacinação de crianças menores pareciam compensar os riscos, outros mostram-se preocupados em concordar com a vacinação baseando-se em estudos realizados apenas em alguns milhares de crianças, refere a agência Reuters nesta quarta-feira.
Para esta vacina, a Pfizer reduziu o conteúdo para um terço da dose adulta. Segundo a farmacêutica, os ensaios clínicos mostraram que a dose mais baixa protegeu bem as crianças contra infeções sintomáticas. E a esperança é que cause menos efeitos colaterais.
Ressalvas e considerações
A maior preocupação era o risco teórico de miocardite – doença cardíaca inflamatória observada em algumas pessoas que tomaram as vacinas da Pfizer e da Moderna e mais comum entre os homens jovens (ainda que geralmente de forma leve).
Não foram testadas crianças pequenas em número suficiente para mostrar se também correm risco.
Segundo Arnold Monto, presidente do comité da FDA e professor de epidemiologia da Universidade de Michgan, é expectável que a dose mais baixa utilizada nesta vacina “diminua a frequência do raro efeito colateral das miocardites”.
Obrigação da vacina “seria um erro”
“Estou apenas preocupado com o facto de que, se dissermos sim, os Estados imponham a administração desta vacina para admissão de crianças na escola e eu não concordo com isso”, disse o Dr. Cody Meissner, professor de pediatria da Universidade Tufts Escola de Medicina. “Acho que seria um erro neste momento”, adianta.
Tal hipótese não deverá vingar. Peter Marks, dirigente do Centro de Avaliação e Pesquisa Biológica da FDA – o departamento para as vacinas do regulador norte-americano – considera-a improvável.
Após a votação, o responsável sublinhou que a autorização diz respeito a um “uso de emergência e não de uma aprovação em geral”.
Do lado dos Centros de Controlo e Prevenção de Doenças dos Estados Unidos, Amanda Cohn lembrou ao comité que morreram crianças de Covid-19. De acordo com o CDC, mais de 700 crianças menores de 18 anos morreram com a doença.
Segundo a Pfizer, os testes clínicos mostraram que a vacina é mais de 90% eficaz na prevenção de infeções sintomáticas em crianças.
Próximos passos
A FDA irá agora avaliar a votação do comité, sendo provável que a confirme.
Depois, será a vez de se pronunciarem os consultores dos Centros de Controlo e Prevenção de Doenças (CDC), que se irão reunir nos dias 2 e 3 de novembro e decidir se recomendam a toma da vacina pelas crianças norte-americanas.
A palavra final caberá à diretora Rochelle Walensky. Em caso de luz verde, a vacinação poderá arrancar na semana seguinte.
O governo federal já tem em marcha um plano para a distribuição de vacinas de menor porte por consultórios de pediatras, farmácias e outros locais.
A vacina da Pfizer é autorizada para jovens de 12 a 17 anos, e uma análise da CNN dos dados do CDC mostra que cerca de metade dos adolescentes nessa faixa etária nos Estados Unidos estão totalmente vacinados.