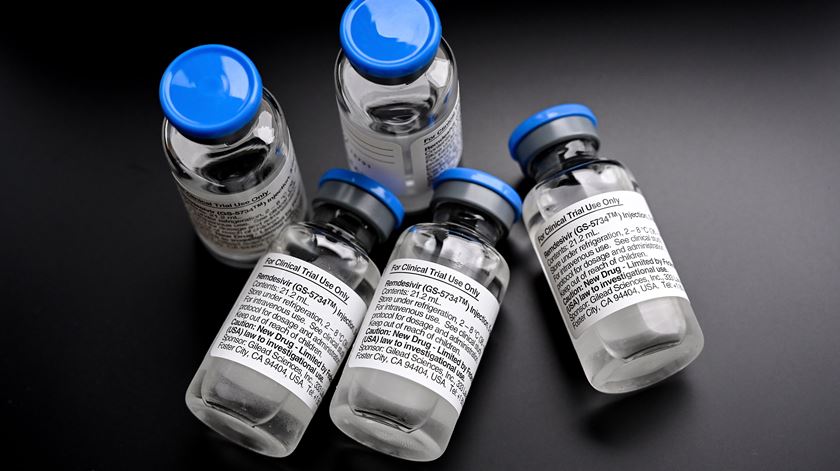
Covid-19: Tratados 133 doentes com remdesivir no SNS
29 jul, 2020 - 14:12 • Joana Gonçalves
A Comissão Europeia anunciou, esta quarta-feira, um investimento de 63 milhões de euros para assegurar tratamentos com Remdesivir na União Europeia (UE).
Veja também:
- Os últimos números da pandemia em Portugal e no mundo
- Todas as notícias sobre a pandemia de Covid-19
- Guias e explicadores: as suas dúvidas esclarecidas
- Boletins Covid-19: gráficos, balanços e outros números
Desde o início da pandemia em Portugal, 133 doentes infetados com o novo coronavírus foram tratados com o medicamento antiviral remdesivir, no SNS. O anúncio foi feito pelo presidente do Infarmed, Rui Ivo, durante a habitual conferência de imprensa da Direção-Geral da Saúde (DGS).
A informação é conhecida no mesmo dia em que a Comissão Europeia anunciou que assinou um contrato de 63 milhões de euros com a farmacêutica Gilead para assegurar tratamentos com Remdesivir na União Europeia (UE).
"A partir do início de agosto, lotes deste medicamento, Veklury [marca comercial do Remedesivir] será disponibilizado aos Estados-Membros e ao Reino Unido. A Comissão coordenará a distribuição desses lotes", anunciou a porta-voz Dana Spinant.
"Este primeiro lote servirá apenas para as necessidades imediatas", afirmou, assegurando que "ao mesmo tempo, a Comissão está também a preparar um contrato conjunto para novas entregas deste medicamento, para cobrir as necessidades adicionais a partir de outubro".
Pandemia de Covid-19
Infarmed assegura que Portugal tem stock e acesso imediato a medicamento remdesivir
Os Estados Unidos compraram à empresa Gilead Scien(...)
De acordo com o presidente do Infarmed, a distribuição será feita em conjugação com o Centro Europeu de Prevenção e Controlo das Doenças (ECDC) e terá como principal critério a situação epidemiológica de cada país. “Neste momento temos quantidades disponíveis no nosso SNS”, garantiu Rui Ivo.
No início de julho, o Remdesivir foi autorizado pela Agência Europeia de Medicamentos (EMA, na sigla inglesa) como o primeiro tratamento da covid-19, visando então curar adultos e adolescentes a partir dos 12 anos de idade com pneumonia que necessitam de oxigénio suplementar.
Enquanto estiver autorizado para ser comercialização para tratamento da covid-19 na UE, o medicamento continua a ser monitorizado para garantir a sua segurança.
À Gilead foi ainda solicitado que apresente até final do ano relatórios finais dos estudos Remdesivir à EMA, sendo esta uma das condições a cumprir para passar de uma autorização condicional de introdução no mercado para uma autorização total.